外显子组测序可预测是否对免疫疗法有反应
发布日期:2022-07-21免疫疗法例如免疫检查点抑制剂,已经改变了晚期癌症的治疗。与杀死癌细胞的化学疗法不同,这些药物可帮助人体的免疫系统,自行发现并摧毁癌细胞。不幸的是,只有一部分患者对免疫检查点抑制剂有长期反应,而这些治疗方法的成本很高,而且有副作用。
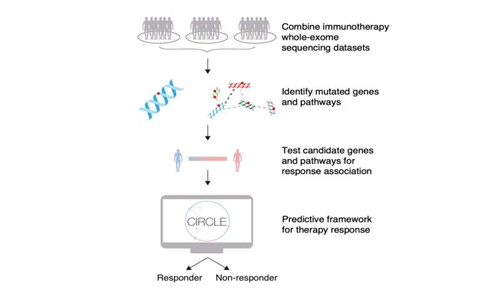
研究人员开发了一种两步方法,使用全外显子组测序将预测癌症患者、是否会对免疫疗法产生反应的基因和途径归零。该研究发表在《自然通讯》杂志上,由纽约大学、威尔康奈尔医学中心和纽约基因组中心的研究人员进行,说明了与目前的实验室测试相比,使用全外显子组测序可以更好地预测治疗反应。
“我们能更好地预测,谁将从免疫疗法中受益吗?科学家们已经开发出各种生物标志物来帮助预测免疫疗法的治疗反应,但仍然需要一个强大的、临床实用的预测模型,”纽约大学生物学助理教授 Neville Sanjana 说。
已知一些生物标志物——包括年龄、肿瘤类型和癌细胞中发现的突变数量(称为肿瘤突变负荷),与对免疫疗法的反应相关。通过分析数百个基因计算出的肿瘤突变,负担是最完善的预测因子,通常用于确定患者是否有资格使用免疫检查点抑制剂。如果科学家研究我们基因的更大部分,这是否有助于更好地预测哪些患者会对免疫疗法产生反应?
全外显子组测序是一种对编码蛋白质的基因组部分进行测序的方法——大约 20,000 个基因,或基因组的 2%,以寻找可能与疾病有关的突变。虽然全外显子组测序并未广泛用于癌症治疗,但一些免疫疗法研究已开始包括测序,这些研究规模虽小,但共同有助于阐明基因组因素与患者对免疫疗法的反应之间的关系。
研究人员结合了先前对黑色素瘤、肺癌、膀胱癌和头颈癌患者的六项免疫治疗研究的数据。所有接受免疫检查点抑制剂(抗 PD-1 或抗 CTLA-4)治疗的参与者均可使用全外显子组测序。但即使将这六项研究结合起来,患者的数量——总共 319 人仍然相对较少。“只有几百人的小型研究的问题是,患者数量与全外显子组测序中测序的大量基因之间的不匹配。理想情况下,我们的数据集包含的患者多于基因,”Zoran Gajic 说。
为了解决这个问题,研究人员转向了一种名为 fishHook 的模型,该模型将导致癌症的突变与背景突变或偶然发生、但与癌症无关的突变区分开来。该模型,校正了一系列影响背景突变率的因素,例如调整基因的大小,因为较大的基因更有可能发生突变。





