COVID疫苗背后的技术,可适于癌症疫苗
发布日期:2021-09-11牛津大学和路德维希癌症研究所的科学家正在牛津-阿斯利康针对 SARS-CoV-2 疫苗的成功基础上开发一种治疗癌症的疫苗。研究人员使用牛津大学的病毒载体疫苗技术设计了一种两剂治疗性癌症疫苗。
在小鼠肿瘤模型中进行测试时,癌症疫苗增加了浸润肿瘤的抗肿瘤 T 细胞的水平,并提高了癌症免疫疗法的功效。与单独的免疫疗法相比,与疫苗的组合显示出更大的肿瘤尺寸减小并提高了小鼠的存活率。这项研究由牛津大学路德维希癌症研究所的 Benoit Van den Eynde 教授小组与共同作者 Adrian Hill 教授、和大学詹纳研究所的 Irina Redchenko 博士合作完成,发表在癌症免疫治疗杂志。
癌症免疫疗法——让患者自身的免疫系统对抗肿瘤,已经显着改善了一些癌症患者的治疗效果。抗PD-1 免疫疗法的工作原理是让抗肿瘤 T细胞刹车,让它们杀死癌细胞。然而,尽管取得了这一成功,但抗 PD-1 疗法对大多数癌症患者无效。抗 PD-1 癌症治疗效果不佳的原因之一是,一些患者的抗肿瘤 T 细胞水平较低。牛津大学的疫苗技术用于创造世界著名的牛津-阿斯利康 COVID-19 疫苗,可产生强大的 CD8+ T 细胞反应,这是获得良好抗肿瘤效果所必需的。
该团队开发了一种具有不同初始和加强病毒载体的两剂治疗性癌症疫苗,其中一种与牛津-阿斯利康 COVID-19 疫苗中的载体相同。为了创造一种专门针对癌细胞的疫苗治疗,该疫苗旨在针对存在于多种类型癌细胞表面的两种 MAGE 型蛋白质。这两个目标被称为 MAGE-A3 和 NY-ESO-1,之前已经过路德维希研究所的验证。
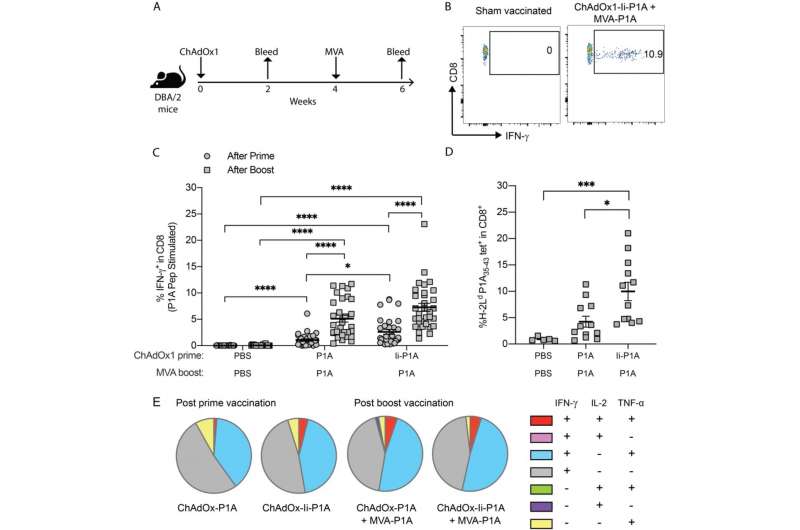
小鼠肿瘤模型的临床前实验表明,癌症疫苗增加了肿瘤浸润性 CD8+ T 细胞的水平,并增强了对抗 PD-1 免疫疗法的反应。与单独的抗 PD-1 治疗相比,联合疫苗和抗 PD-1 治疗导致肿瘤大小更小,并提高了小鼠的存活率。
牛津大学肿瘤免疫学教授、路德维希癌症研究所成员兼比利时德杜夫研究所所长 Benoit Van den Eynde 说:“我们从之前的研究中了解到 MAGE 型蛋白质的作用,类似于红色癌细胞表面的标记,以吸引破坏肿瘤的免疫细胞。
MAGE 蛋白作为疫苗靶点比其他癌症抗原更具优势,因为它们存在于多种肿瘤类型中。这扩大了这种方法对患有许多不同类型癌症的人的潜在益处。“对于靶标特异性很重要,正常组织表面不存在 MAGE 型抗原,这降低了免疫系统攻击健康细胞引起的副作用风险。”





