消除RNA结合蛋白可提高白血病的存活率
发布日期:2021-08-06加州大学洛杉矶分校琼森综合癌症中心的科学家领导的一项小鼠研究表明,去除一种经常在罕见且侵袭性亚型白血病中过度表达的蛋白质,有助于减缓癌症的发展并显着增加存活的可能性。
这项研究,今天在杂志上发表白血病,可在靶向治疗的发展援助是有高水平的RNA结合蛋白IGF2BP3,尤其是急性淋巴细胞和粒细胞白血病,在混合系的特点是染色体重排的癌症白血病(MLL)基因。在这些MLL重排的白血病中,IGF2BP3附着在某些携带癌症相关蛋白遗传指令的RNA分子上,显着放大了癌症的发展。诊断为该亚型的儿童和成人预后不良,治疗后复发风险高。
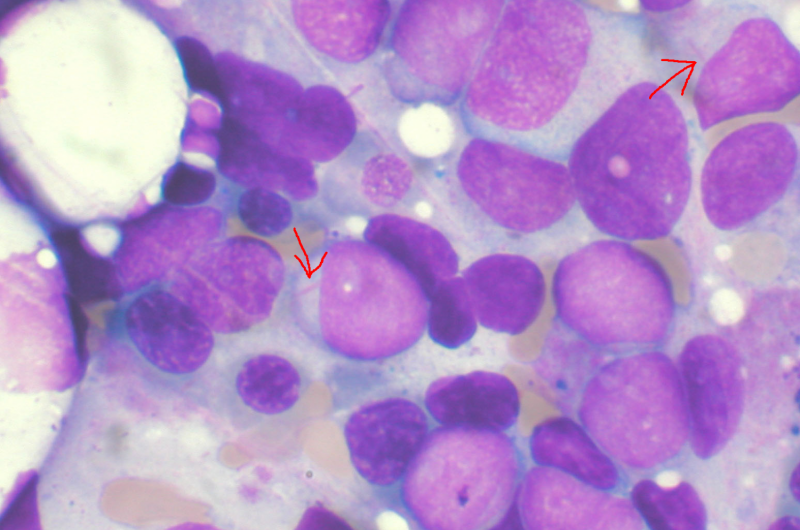
“这种类型的白血病更具侵袭性,因为它能够更快地分裂和扩散,”资深作者、琼森癌症中心成员、大卫格芬医学院病理学和实验室医学副教授DineshRao博士说。在加州大学洛杉矶分校,“这种疾病可能非常难以治疗,即使采用新的靶向免疫疗法,如CART细胞疗法和blinatumomab。”
白血病始于骨髓,由基因突变引发,导致骨髓中的干细胞产生过多的白细胞,影响身体抵抗感染的能力。Rao和他的团队早些时候通过调节导致疾病的各种RNA信息,将IGF2BP3确定为推动白血病发展的一个因素,尤其是MLL重排亚型。
考虑到这一点,研究人员想知道去除IGF2BP3蛋白是否可能阻止白血病细胞的增殖。为了回答这个问题,Rao和他的团队使用强大的基因编辑工具CRISPR-Cas9从MLL白血病小鼠和细胞系中去除IGF2BP3。他们发现,对生存的影响是惊人的。
在IGF2BP3缺失的白血病小鼠中,大约75%的总存活率增加,50%没有白血病。研究小组还观察到,在去除IGF2BP3后,小鼠的肿瘤负荷(体内肿瘤组织的总质量)平均减少了四倍,以脾脏的重量衡量。
“这些结果确实突出了IGF2BP3作为一个有吸引力且有价值的治疗靶点,”主要作者、加州大学洛杉矶分校分子、细胞和综合生理学跨部门博士项目的研究生研究员TiffanyTran说。“通过靶向这种RNA结合蛋白,我们将能够直接靶向癌细胞,而让健康的非癌细胞单独存在。”
在靶向IGF2BP3时,该团队还发现该蛋白质对于小鼠的正常血液发育不是必需的。去除蛋白质后,血液系统几乎完好无损。即使是完全缺乏这种蛋白质的小鼠也能正常发育。“这让我们感到惊讶,因为许多在癌症中很重要的蛋白质在正常组织中也很重要,”Rao说,他也是UCLAEli和EdytheBroad再生医学和干细胞研究中心的成员。
“这也是一个有吸引力的目标,因为我们在理解它如何在癌细胞中发挥作用方面取得了一些真正的进展,”Rao补充道。“我们能够确定它结合的一些重要的RNA分子,这些分子编码其他致癌蛋白。所以如果你能去除这种蛋白质,你就能够改变其他致癌蛋白的数量。”
虽然该团队研究了IGF2BP3作为MLL白血病的靶点,但该蛋白质也在约15%至20%的其他癌症类型中高度表达,包括胶质母细胞瘤、胰腺癌、肺癌和黑色素瘤。研究人员的下一步是了解去除蛋白质,是否对其他类型的癌症具有同样强的作用,以及开发基于小分子和RNA的疗法、来尝试干扰蛋白质的功能。





