赴美看病 患者如何获得临床试验药物
发布日期:2017-12-07什么是试验性药物?
试验性药物是处于研究阶段,没有获得美国食品和药物管理局(FDA)许可,未能获批在美国合法销售的药物。FDA批准是药物开发过程的后一步。第一步是在实验室里测试新药。如果结果积极,下一步是开展人体药物试验,在此之前,药物公司或赞助商须向FDA提出申报。这称为新药临床试验(IND)。一旦IND被批准,临床试验即可开始。临床试验研究是为了确定药物的安全性和有效性。
赴美看病机构爱诺美康介绍,临床试验完成后,发起人把研究结果以新药申请或生物制剂许可申请的形式提交FDA。经过仔细审查,如认为申请的药物是安全有效的,终就会获得批准。
患者有什么途径可以获得试验性药物?
目前为止,病人获取试验药物常见的方式是参加临床试验,医生可能会建议将试验药物纳入治疗方案,患者及家属可向医生咨询临床试验或治疗癌症的新药。患者及家属也可以通过检索美国国家癌症研究所NCI的临床试验数据库(如下图),来获取更多有关进行中的临床试验新药的信息。
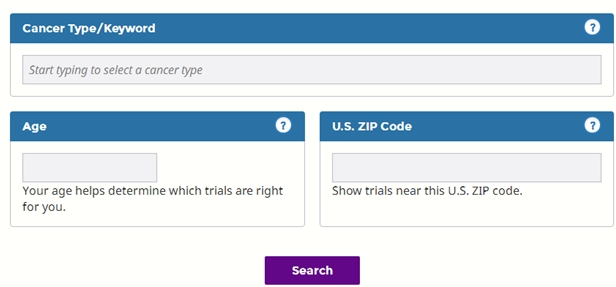
此外还有其他方式获得试验药物吗?
不太常用的方式包括诸如扩展访问协议、特殊情况或同理心优先特例。赴美看病机构爱诺美康介绍,临床试验发起人必须同意药物经此途径使用,这些例外机制下的试验药物,必须符合下列标准:1、必须有大量的临床证据表明该药物可以让特定癌症的人群受益。2、必须能在临床试验之外安全给药。3、必须保证对正在进行和计划进行的临床试验有足够的药物供应量。
所有的试验药物都能够通过扩展访问协议,或特殊的例外机制来获得吗?
不,发起人有权决定是否在临床试验以外提供试验药物,其可行性在一定程度上受到药物供应、患者需求或其他因素的制约。
如果可以通过临床试验之外的方式使用药物,判断患者能否接受治疗的标准有哪些?
患者必须符合以下标准:1、曾接受标准疗法但疗效不佳。2、不适合任何正在进行的临床试验。3、没有可接受的治疗方案。4、试验药物对此种癌症表现出活性。5、预计获益多于风险。
想通过特殊的例外机制来接受试验药物,该怎么办?
对获得试验药物感兴趣的病人应向医生咨询可行的选择。医生可以与研究发起人联系,从而提出特殊的例外机制的请求。此过程中要求医生遵守严格的指导方针,包括取得机构审查委员会的批准,并获得病人的知情同意。知情同意书需由病人签署,其中概述了治疗的已知风险和益处,以及病人的权利和责任。
接受试验药物的费用是多少?
赴美看病机构爱诺美康介绍,一般来说,试验药物是免费提供的。然而,治疗可能会产生其他费用,开始治疗前,患者应与保险公司核对费用的相关情况。
接受试验药物的潜在缺点有哪些?
目前尚不清楚试验药物是否优于标准疗法,不排除病人可能无法受益。对于药物的副作用(包括长期和短期)无法完全理解,尤其是当药物还处于早期测试阶段。另外,健康保险可能不涵盖试验药物相关的费用。





