研究人员为食管癌生成了实验培育的组织模型
发布日期:2022-12-22通过使用CRISPR/Cas9基因编辑技术对关键肿瘤抑制基因(TP53/CDKN2A)进行双敲除,修饰了人胃食管连接衍生的类器官,这导致细胞变得更加癌变。
根据美国癌症协会的数据,全世界每年有100多万人死于胃食管癌,近几十年来,GEJ癌症的发病率增加了两倍多,每年新增50万至100万例。胃酸反流、吸烟和胃幽门螺杆菌感染是食管和胃肿瘤的公认危险因素。
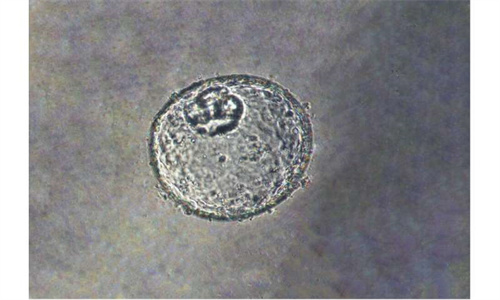
但专家表示,很难证明癌症是如何从胃和食道的交界处开始的,部分原因是缺乏与GEJ生物学相关的早期疾病模型。“因为我们没有一个独特的模型来区分GEJ肿瘤,胃食管癌通常被归类为食管癌或胃癌,而不是GEJ癌。”
“我们的模型不仅有助于确定GEJ肿瘤生长过程中发生的关键变化,还为未来的研究建立了策略,以帮助了解其他器官的肿瘤。”而类器官包括由干细胞衍生的三维细胞集合,这些细胞可以复制器官的特征或器官的功能,例如制造特定种类的细胞。
研究人员使用一种基因编辑技术,即簇状规则间隔的回文重复序列(CRISPR/Cas9),敲除了类器官中的两个关键肿瘤抑制基因(TP53和CDKN2A)。这些基因的双重敲除导致细胞变得更加癌变,生长更加迅速,显微特征更接近恶性。这些改变的类器官,也在免疫缺陷小鼠中形成肿瘤。





