UCLA开发新型免疫疗法,有望改写子宫内膜癌治疗格局
发布日期:2026-05-09加州大学洛杉矶分校(UCLA)研究团队开发出一种名为 CAR-NKT 的新型免疫细胞疗法,在子宫内膜癌临床前模型中实现了肿瘤完全清除,且对侵袭性亚型效果尤为突出。该疗法仍处于临床前阶段,但已完成全部实验室验证,正准备向美国FDA提交临床试验申请。
背景:子宫内膜癌,一个被忽视的"沉默危机"
子宫内膜癌是美国最常见的妇科恶性肿瘤。令人担忧的是,近几十年来其生存率不升反降。
更严峻的数据在于疾病的高度异质性:
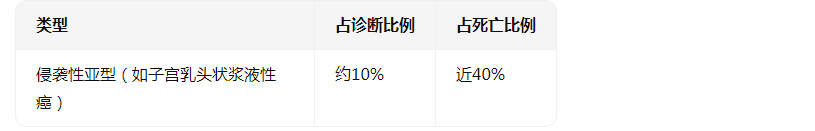
也就是说,仅一成的患者,贡献了四成的死亡。现有治疗手段对这类侵袭性亚型效果有限,复发率居高不下——这正是新疗法瞄准的核心痛点。
核心技术:CAR-NKT——比CAR-T多两条"攻击路径"
1. 它是什么?
CAR-NKT疗法使用的是一种特殊免疫细胞——不变自然杀伤T细胞(iNKT细胞),通过基因工程为其装上"嵌合抗原受体"(CAR),使其能精准识别并攻击癌细胞。
2. 靶点:间皮素(Mesothelin)
研究团队选择的靶标是间皮素——一种在子宫内膜癌细胞表面高度表达的蛋白质。这一选择并非偶然:间皮素还广泛存在于卵巢癌、乳腺癌、胰腺癌和肺癌中,意味着该疗法未来可能"一药多癌"。
3. 关键优势:三路同时出击
与传统CAR-T细胞依赖单一识别机制不同,CAR-NKT细胞具备三条并行的肿瘤杀伤通路:
通路一:CAR介导的靶向识别(精准锁定间皮素)
通路二:NKT细胞天然的细胞毒活性
通路三:免疫调节功能(激活其他免疫细胞协同作战)
研究人员认为,正是这种"多线作战"的设计,大幅降低了肿瘤通过单一通路逃逸的可能性——这恰恰是复发的根源。
实验室数据:完胜传统CAR-T
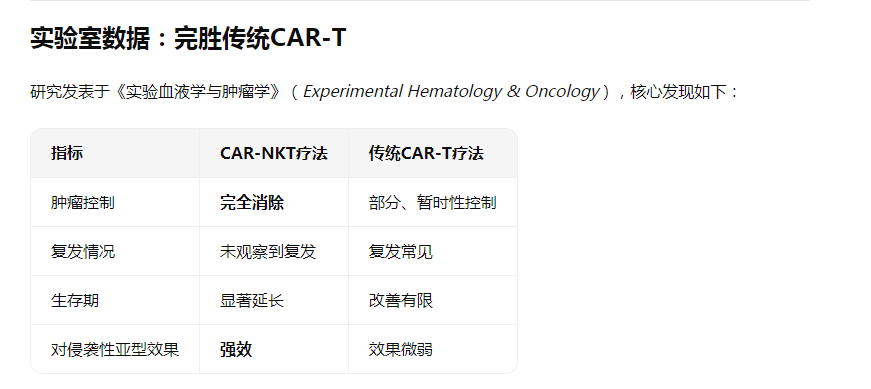
此外,在患者来源的肿瘤样本和肿瘤细胞系上进行的额外测试也证实:CAR-NKT的抑癌活性全面优于现有免疫疗法,包括对子宫乳头状浆液性癌这一"硬骨头"。
现成平台:不用等、不用贵、不用配型
这可能是该疗法最具颠覆性的特征之一。
现有CAR-T的痛点
个性化生产:需采集患者自身免疫细胞→体外改造→回输,周期长达数周
成本高昂:单次治疗费用可达数十万美元
供应链脆弱:每例都是"定制款",产能受限
CAR-NKT的破局之道
通用型(Off-the-shelf):使用捐赠者的血液干细胞,通过可扩展工艺批量生产
天然相容性:iNKT细胞与不同个体的免疫系统天然兼容,一次捐赠可制备数千次治疗所需的细胞
即取即用:细胞可预先制备、冷冻保存,患者需要时直接解冻使用
简单比喻:传统CAR-T像"高级定制西装",CAR-NKT像"优衣库爆款"——好穿、便宜、随时有货。
安全性:临床前模型未见重大风险
免疫疗法最怕的副作用之一是移植物抗宿主病(GVHD)——供体免疫细胞反过来攻击患者健康组织,严重时可致命。
好消息是:
✅ 临床前模型中未观察到GVHD
✅ 未报告其他明显安全问题
⚠️ 但必须强调:尚未进入人体试验,安全性和有效性仍需临床验证
下一步:距人体试验仅一步之遥
研究团队已完成全部临床前研究,目前正在准备向美国FDA提交IND(新药临床试验申请)。如果审批顺利,预计未来1–2年内可启动首次人体试验。
潜在影响:不只是子宫内膜癌
由于靶点间皮素在多种实体瘤中高表达,该疗法的适用范围可能远超子宫内膜癌:
卵巢癌
三阴性乳腺癌
胰腺癌
非小细胞肺癌
间皮瘤
如果临床试验成功,同一款产品有望覆盖多种难治性癌症,这在免疫疗法领域极为罕见。





